针对无特定驱动基因突变的IV期非小细胞肺癌(NSCLC)的治疗策略,正处于持续而深刻的演进之中。美国临床肿瘤学会(ASCO)发布的2026.3.0版动态指南,整合了截至2025年10月的最新临床试验证据,为这一复杂领域的临床决策提供了关键更新[1],特别是其在一线治疗分层、后线治疗革新以及未来治疗模式探索方面的进展。
PART1一线治疗:基于PD-L1表达的精准分层与策略权衡
新版指南进一步巩固了PD-L1表达作为一线治疗决策核心生物标志物的地位。治疗策略的选择不再是简单的方案罗列,而是基于不同PD-L1表达水平下,对疗效、毒性及患者特征的综合权衡。
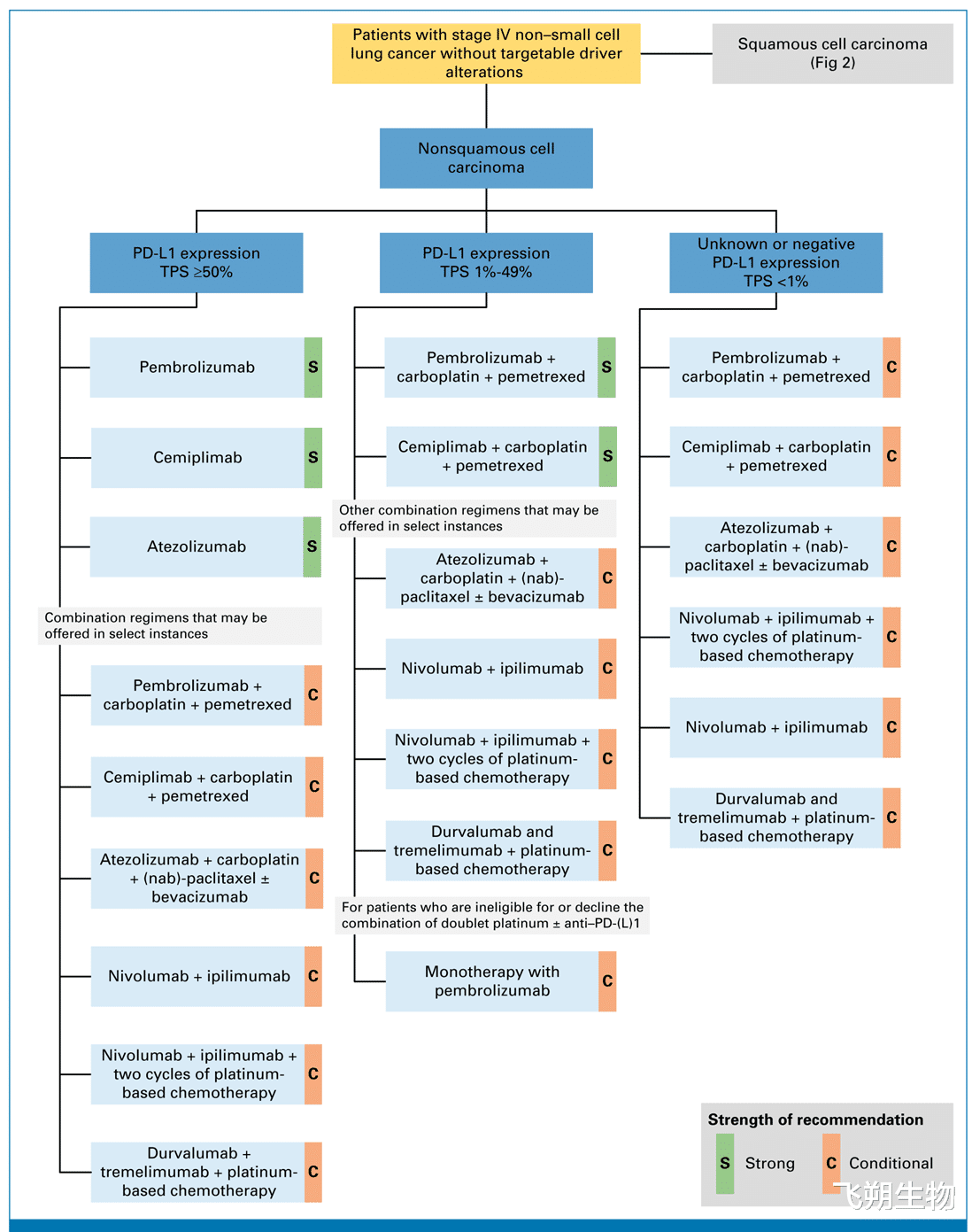
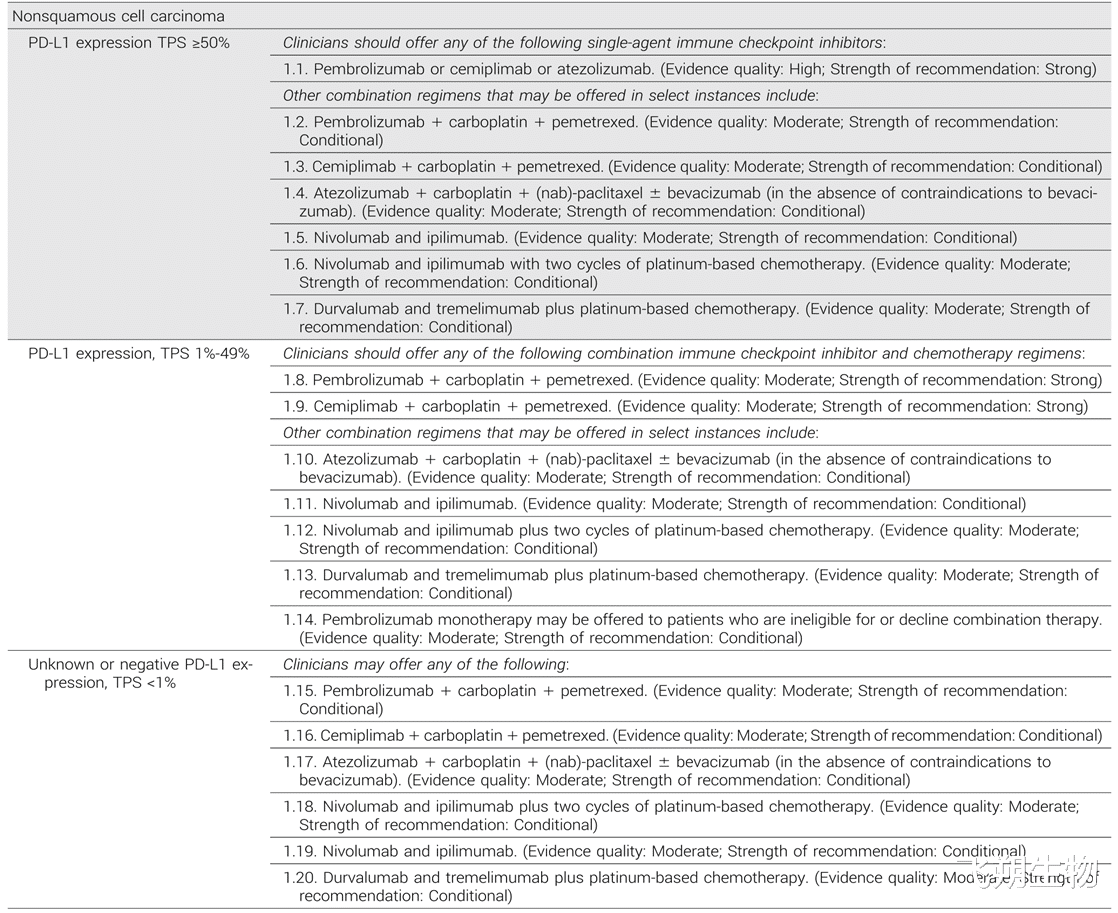
▲IV期无驱动突变非小细胞肺癌及非鳞状细胞癌患者的一线治疗方案
对于证据等级与推荐强度相同的多种治疗方案推荐方案,应根据患者个体疗效与毒性评估结果制定具体用药方案。nab:纳米颗粒白蛋白结合型;NSCLC:非小细胞肺癌;PS:体能状态;TPS:肿瘤比例评分。
1. PD-L1 TPS ≥50%:免疫单药基石地位的再确认
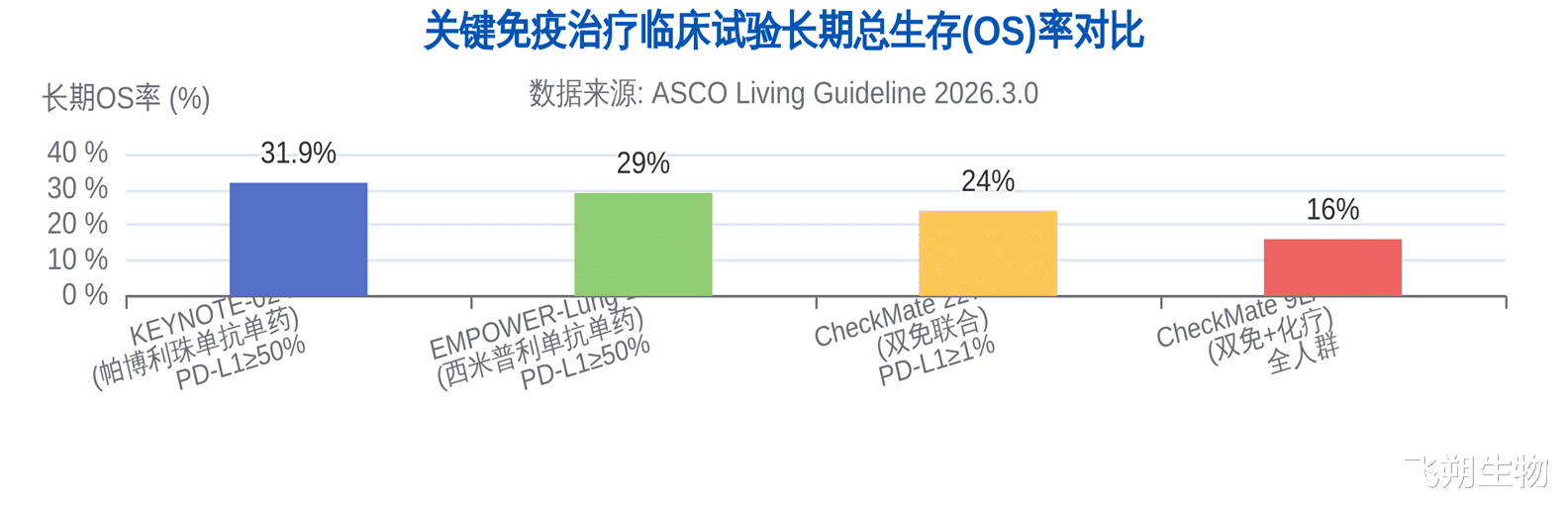
对于PD-L1高表达人群,指南以“强推荐”级别重申了PD-(L)1抑制剂单药治疗(帕博利珠单抗、西米普利单抗或阿替利珠单抗)的基石地位。这一推荐的底气源于多项III期临床试验令人信服的长期生存数据。例如,KEYNOTE-024研究的5年随访显示,帕博利珠单抗单药治疗的OS率达31.9%[2];同样,EMPOWER-Lung 1研究中西米普利单抗的5年OS率也达到了29.0%[3]。这些数据确立了免疫单药在该人群中的疗效标杆。
值得注意的是,指南并未将联合化疗或双免方案作为此亚组的优先推荐。其背后的临床考量是:尽管联合方案(如KEYNOTE-189/407)在PD-L1高表达亚组中同样显示OS获益,但目前缺乏直接证据表明其优于单药治疗。更重要的是,联合治疗势必增加毒性风险。因此,在缺乏明确的疗效升级证据时,避免不必要的治疗增负是重要的临床原则。仅对于肿瘤负荷高、症状重或存在内脏危象风险的特定患者,临床医生可考虑联合化疗以追求更高的客观缓解率和更快的肿瘤退缩。
2. PD-L1 TPS 1%-49%:免疫联合化疗的标准范式
对于PD-L1低表达患者,免疫检查点抑制剂联合铂类双药化疗的模式已成为无可争议的标准治疗。KEYNOTE-189研究的5年数据显示,在非鳞癌PD-L1 1-49%亚组中,帕博利珠单抗联合化疗组的5年OS率高达19.8%,而单纯化疗组仅为7.7%[4]。相似的结论在EMPOWER-Lung
3研究中也得到验证,西米普利单抗联合化疗显著改善了生存(HR=0.50),进一步夯实了该联合策略的循证医学基础。
3. PD-L1 TPS <1%:多元化联合策略的探索与博弈
PD-L1阴性人群的治疗是当前最具挑战和探索性的领域。指南提供了多种“条件性推荐”方案,反映了不同策略间的疗效与毒性博弈。
免疫+标准化疗:作为基础选项,其有效性在KEYNOTE-189等研究的PD-L1阴性亚组中得到证实,5年OS率(9.6% vs 5.3%)虽有改善,但绝对获益有限。
双免+有限化疗:CheckMate 9LA方案(纳武利尤单抗+伊匹木单抗+2周期化疗)为此亚组带来了重要启示。其设计理念在于通过短期化疗快速控制肿瘤,同时利用双免协同作用激发持久的免疫应答。最终分析显示,在PD-L1阴性人群中,该方案的6年OS率达到20%,远超单纯化疗的7%,其“长尾效应”尤为突出[5]。
四药联合方案:POSEIDON研究探索了度伐利尤单抗+曲美木单抗+化疗的模式,同样观察到生存获益趋势,为临床提供了又一选择。
临床决策需在患者的体能状态、合并症以及对不同毒性谱的耐受能力之间进行精细权衡。
对于经含铂化疗和免疫治疗后进展的患者,传统的多西他赛(±雷莫西尤单抗)方案疗效有限。2026版指南的一个重大转变,是将两款ADC药物纳入推荐,标志着即使在无“经典”驱动基因突变的NSCLC中,后线治疗也开始迈向基于蛋白表达的精准靶向时代。
后线治疗新增推荐(条件性):
Telisotuzumab vedotin (Teliso-V):针对c-MET蛋白高表达(定义为≥25%肿瘤细胞呈3+强度)的患者。LUMINOSITY试验显示,该人群的ORR为34.6%,中位OS达14.6个月,提供了有价值的治疗选择[6]。
Trastuzumab deruxtecan (T-DXd):针对HER2过表达(IHC 3+)的患者。综合DESTINY-Lung01/03研究数据,在5.4 mg/kg剂量下,ORR可达34.1%-44.4%,中位OS为11.2-17.1个月,显示出明确的临床活性[7]。
这一更新的临床意义在于,它要求临床医生在患者后线治疗失败时,重新考虑进行组织活检或利用已有样本进行c-MET和HER2的免疫组化(IHC)检测,从而为患者寻找新的治疗机会。
PART3未来方向:治疗模式的演进与新机制的探索指南的“未来研究”部分,前瞻性地指出了两个将深刻影响临床实践的方向。
1.皮下注射(SC)剂型:优化治疗体验与医疗资源配置
帕博利珠单抗和阿替利珠单抗的皮下注射剂型在III期研究(3475A-D77和IMscin001)中,均证明了其在药代动力学、疗效和安全性上不劣于静脉剂型。其核心优势在于显著缩短了患者的院内治疗时间(“座椅时间”减少近50%)[8]。这不仅改善了患者的治疗体验,也为优化医疗资源配置、提高医疗系统运行效率提供了可行路径。
2. VEGF/PD-1双特异性抗体:挑战现有标准
指南对在中国进行的HARMONi-2研究给予了特别关注。该研究中,依沃西单抗(Ivonescimab),一种VEGF/PD-1双特异性抗体,在一线治疗PD-L1阳性NSCLC时,其PFS显著优于帕博利珠单抗,并观察到OS获益趋势[9]。这一结果提示,协同阻断VEGF和PD-1通路可能带来超越单靶点抑制的临床获益,对现有的一线治疗标准构成了潜在挑战。其全球多中心研究的结果值得高度期待。
PART4临床启示2026.3.0版ASCO动态指南的核心,是从“分层治疗”向“精准分层治疗”的深化。在一线,PD-L1表达的定量评估指导着免疫单药、免疫联合化疗或更复杂联合模式的选择与权衡。在后线,c-MET和HER2等蛋白表达水平正成为新的生物标志物,引领ADC药物进入临床实践。此外,指南再次强调了在疾病早期即整合跨学科姑息治疗(包括创新的远程医疗模式)的重要性,这对于全面提升患者生活质量和改善总体生存具有不可估量的价值。
参考文献
[1] J Clin Oncol. 2026 Mar;44(7):e56-e88.
[2] J Clin Oncol. 2021;39:2339-2349.
[3] J Thorac Oncol. 2025;20:941-954.
[4] J Clin Oncol. 2023;41:1992-1998.
[5] ESMO Open. 2025;10:105123.
[6] J Clin Oncol. 2024;42:3000-3011.
[7] Lancet Oncol. 2024;25:439-454.
[8] Ann Oncol. 2025;36:775-785.
[9] Lancet. 2025;405:839-849.
声明:本文仅用于分享,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!