前言
介入治疗是一门新兴的临床学科,是微创医学的重要组成部分,独立于临床传统内科学和外科学之外的第三大临床学科。介入治疗在不开刀暴露病灶的情况下,借助先进的影像设备(如DSA、B超、CT等)在皮肤上作直径几毫米的微小通道,将特殊的穿刺针、导管等插到病变器官、组织,通过穿刺针或导管直接注入药物、栓塞剂或置入支架等方式对多种疾病进行治疗。为给广大同道提供肝病介入治疗的前沿进展,《国际肝病》携手四川大学华西医院罗薛峰副教授共同创办“国际肝病-介愈肝胆”栏目,每月定时分享介入领域的最新研究,传达规范治疗理念,追踪介入治疗的最新动态,以期对相关领域专家、研究人员及一线医务工作者的研究或工作有所裨益。
介愈肝胆丨小直径亚扩张新辅助TIPS为肝硬化伴临床显著门静脉高压患者拓展肝外肿瘤手术机会重要研究结果分析及其临床意义
研究背景门静脉高压是肝硬化患者围手术期管理的关键限制因素。由于存在临床显著门静脉高压(CSPH),相当一部分本具根治机会的实体肿瘤患者被排除在外科治疗之外,但这一人群规模及其对肿瘤学结局的影响尚未得到充分量化。既往研究已明确,CSPH相关的高动力循环和门体侧支形成可显著增加术中出血、术后腹水及肝功能失代偿风险;在代偿期肝硬化患者接受择期肝外手术时,HVPG、ASA分级及手术方式均为独立死亡预测因素。
基于降低围手术期风险的需求,术前经颈静脉肝内门体分流术(TIPS)作为一种门静脉减压策略逐渐受到关注。然而,传统8-10 mm充分扩张TIPS虽可有效降低门脉压力,却以较高的肝性脑病及心脏负荷风险为代价,限制了其作为常规新辅助策略的推广。近年来,≤7 mm欠扩张TIPS被提出有望在维持有效减压的同时降低分流相关并发症风险(D. Roccarina et al. Hepatology. 2025)。
2026年Liver International发表的一项多中心研究系统评估了亚扩张新辅助TIPS(U.N-TIPS)在合并CSPH的肝硬化患者中的应用价值,结果显示该策略可在可接受安全性下显著提高患者进入肝外肿瘤根治性手术路径的比例,提示“精准减压”可能成为围手术期门静脉高压管理的重要发展方向。尽管如此,其最佳适用人群及长期获益仍有待前瞻性研究进一步验证。
研究设计本研究为一项来自意大利的多中心、回顾性研究,纳入标准包括:依据临床病史、组织学结果以及超声、CT或MRI评估的肝脏形态学特征确诊为肝硬化;确诊存在肝外实体恶性肿瘤;因CSPH(无论是否存在失代偿)而转诊行TIPS,且TIPS的目的为实现根治性肿瘤手术;对于无食管胃静脉曲张的代偿期患者,临床需通过HVPG测量证实其存在窦性CSPH;TIPS置入后腹水完全消失(无论是否仍需利尿剂治疗);术后随访时间不少于6个月。
排除标准包括:TIPS指征与外科手术指征相互独立、因肝细胞癌(HCC)治疗而行肝脏手术、存在TIPS禁忌证(包括重度肝功能衰竭[Child-Pugh评分>11、血清胆红素>3 mg/dL、MELD评分>18]、严重器质性肾功能衰竭、既往心力衰竭病史、左心室射血分数<50%、中重度主动脉瓣狭窄),以及在充分治疗后仍反复或持续存在的显性肝性脑病。研究筛选284例患者,最终纳入34例(12%)(图1)。

图1. 研究人群流程图
所谓“亚扩张TIPS(U.N-TIPS)”,是指通过球囊扩张肝实质内通道及覆膜支架,使其直径小于8 mm,扩张范围包括门静脉及肝静脉。TIPS使用可扩张的聚四氟乙烯(PTFE)覆膜支架(2020年前使用GORE VIATORR SG VTS,2020年起使用GORE VIATORR SG CX 8-10 mm型号)。
本研究的主要终点是评估U.N-TIPS在肝硬化合并CSPH患者中,是否能够成功促成原本因门静脉高压而被排除的择期肝外肿瘤外科手术。次要终点包括围手术期并发症的发生情况、术后显性肝性脑病(OHE)及心力衰竭的发生,以及TIPS术后6个月、1年的生存率。
研究结果01
患者一般特征
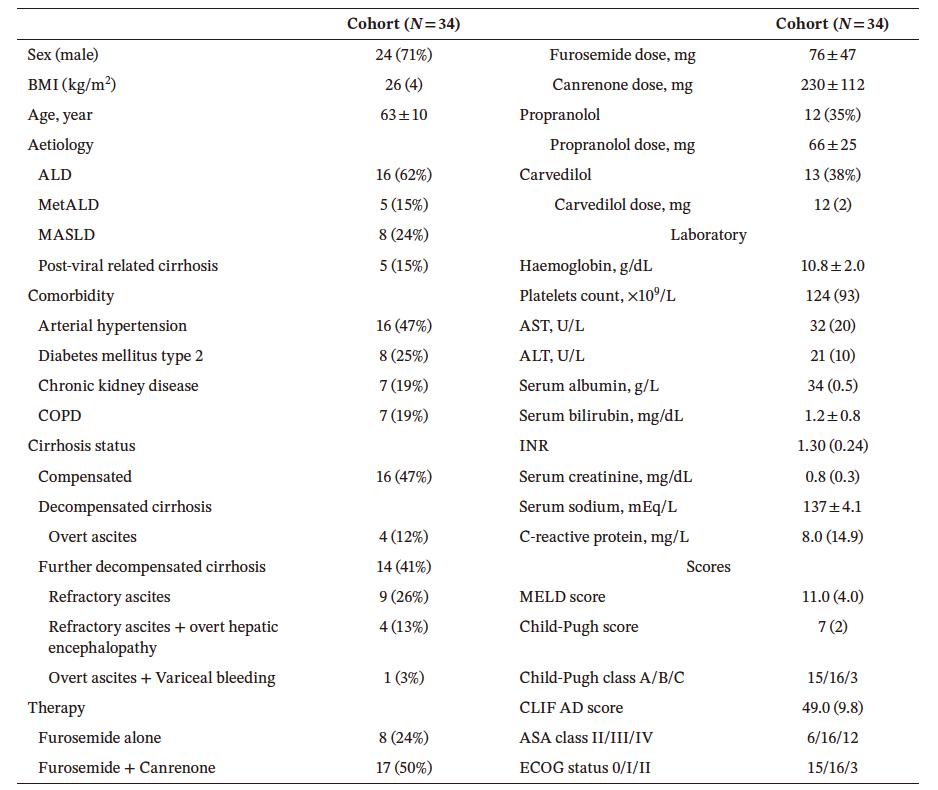
本研究共纳入34例符合U.N-TIPS标准的患者,在肝外恶性肿瘤诊断前,18例患者(53%)至少发生过一次肝脏失代偿事件;25例患者(74%)存在食管静脉曲张(其中代偿期患者占78%,失代偿期患者占69%);24例患者(71%)因腹水形成而接受利尿剂治疗超过3个月;Child-Pugh评分中位数为7分,多数患者属于Child-Pugh B级(47%);MELD评分中位数为11.0分(表1)。
表1. 研究人群的一般特征
02
TIPS及术前临床、实验室与血流动力学评估
在纳入的患者中,分别有10例、17例和7例患者的TIPS被部分扩张至5 mm、6 mm和7 mm。球囊扩张的平均直径为6.5±0.7 mm。PCPG由21±4.5 mmHg显著下降至11±3.2 mmHg(P<0.001),平均降幅为51%±13%(其中,21例患者(62%)PCPG下降≥50%,32例患者(94%)PCPG下降≥30%)。最终支架直径为5/6/7 mm的患者分别为9/17/8例,且所有患者最终均达到PCPG<16 mmHg。在TIPS置入前,8例患者(24%)PCPG为14-16 mmHg(低风险组),7例(20%)为17-19 mmHg(高风险组),19例(56%)≥20 mmHg(极高风险组);TIPS置入后:11例患者不再存在CSPH(平均PCPG 7±2.2 mmHg),21例进入低风险组(平均PCPG 12±1.7 mmHg),2例仍处于高风险组(PCPG均为17 mmHg),无患者仍处于极高风险组(表2和图2)。
表2. TIPS 置入前后的血流动力学指标比较

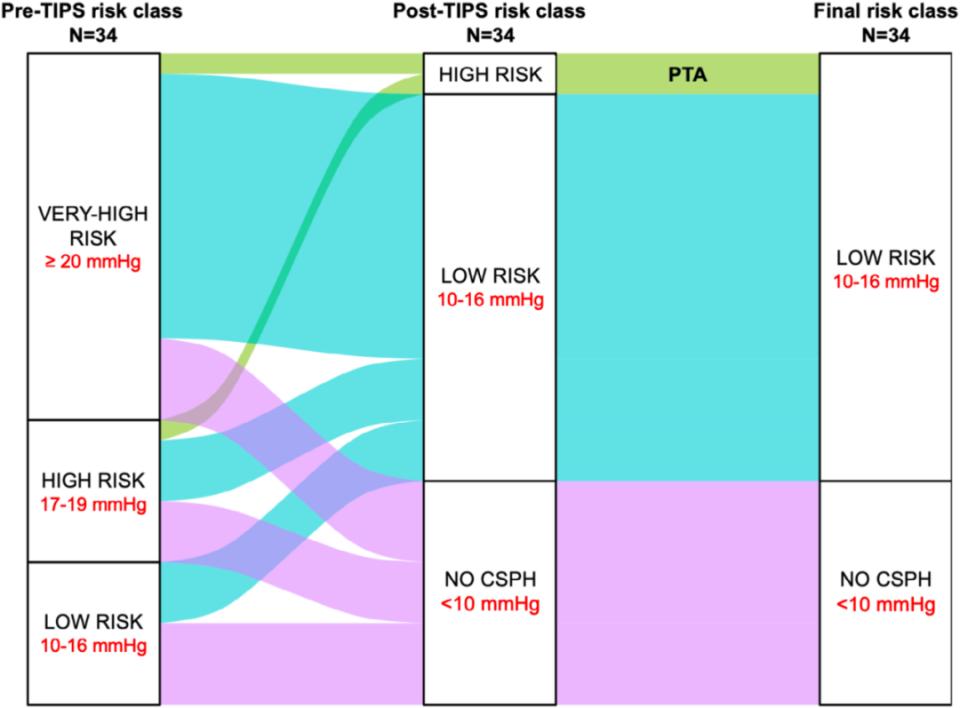
图2. U.N-TIPS患者外科手术风险分级变化图
03
主要终点
TIPS至外科手术的中位间隔时间为42天,失代偿期肝硬化患者的间隔时间显著长于代偿期患者(71天vs.42天;P=0.021);32例(94%)患者成功接受肝外肿瘤外科手术,共2例患者(6%)未接受原计划手术。除1例患者外,其余患者均实现根治性切除(R0切除率97%);总体中位住院时间为12天(表3)。
表3. 纳入患者的癌症诊断、肝病严重程度、CSPH特征及外科计划手术方案


04
次要终点
术后并发症:共有12例患者(38%)发生术后并发症(平均发生时间为术后8±8天),发生术后并发症与未发生并发症患者两组间在TIPS术后PCPG值、手术类型、TIPS前肝硬化状态以及ASA分级方面均未发现显著差异。在单因素和多因素分析中,MELD评分和术前血红蛋白水平被确定为术后并发症的独立预测因素。超过一半的并发症由感染诱发,且多发生于术后早期(中位发生时间5天)。发生并发症的患者住院时间显著延长(20天vs. 9天;P=0.001)。
显性肝性脑病(OHE):共有7例患者在随访期间发生显性肝性脑病(OHE),累计发生率为23%,无持续性病例;另有3例患者在TIPS与外科手术之间发生OHE(平均间隔14±10天),6例患者在外科手术后发生OHE,从TIPS至OHE的平均时间为68±26天,从手术至OHE的平均时间为55±25天。
心力衰竭:共有2例患者(6%)在TIPS术后发生症状性心力衰竭(AHA C级),发生时间距TIPS平均16±5个月,距手术平均15±5个月。其中1例患者因顽固性心衰,于术后410天接受分流道关闭治疗。
TIPS术后生存率:中位随访时间为23.6个月,无患者失访。总体1个月、3个月、6个月及1年生存率分别为97%、88%、85%和76%。在接受外科手术的患者(n=32)中,中位生存期为36.1个月,其1个月、3个月、6个月及1年生存率分别为97%、88%、84%和76%(图3A)。
共有3例患者在术后2个月内死亡(分别于术后第20天、第52天和第54天),其中2例死于感染性休克继发多器官功能衰竭。术后1年时,肿瘤相关死亡率和肝病相关死亡率分别为6%和14%。
TIPS术前为代偿期与失代偿期的患者之间,生存率无显著差异(图3B)。

图3. 接受U.N-TIPS与计划性手术患者的Kaplan-Meier生存分析
VOCAL-Penn评分:在手术前重新计算VOCAL-Penn评分后,预测死亡风险整体向较低水平转移。在标准风险分层(<1%、1%-5%、>5%)中,预测风险越高,与30天、90天和180天死亡率的增加显著相关。在采用20%作为术后肝功能失代偿预测风险阈值时,该评分在术前阶段能够有效区分术后并发症风险显著升高的患者(25% vs. 83%,P=0.014)。
总结本研究是迄今样本量最大的针对肝硬化患者实施新辅助TIPS以促成肝外肿瘤手术的队列研究。研究首次在该临床场景中系统性应用小直径亚扩张覆膜支架策略,结果显示出良好的血流动力学改善效果及令人鼓舞的临床结局。研究中94%的患者最终获得外科手术机会,明显高于既往回顾性研究报道的52%-86%。
既往多数研究同时纳入“为手术目的实施TIPS”以及“因常规指征行TIPS后再接受手术”的患者,队列异质性较大,从而削弱了对新辅助策略真实价值的判断。相比之下,本研究采用严格的个体化决策路径,仅纳入明确以肝外肿瘤手术为目标实施TIPS的患者,使研究人群更加聚焦,也增强了结果的临床解释力。
根据Reverter等基于HVPG的风险分层,HVPG≥20 mmHg显著增加1年术后死亡风险。本研究以PCPG进行分层,58%的患者术前PCPG≥20 mmHg;经U.N-TIPS治疗后,无患者仍处于极高风险组。值得注意的是,即便未将支架扩张至≥8 mm,仍有32%的患者达到PCPG<10 mmHg(即无CSPH),68%进入低风险血流动力学区间,提示“有限分流”亦可获得充分减压效果。
围手术期方面,38%的患者出现术后并发症,其中超过一半由院内感染诱发,而未观察到显著术中出血事件。基线失代偿状态及手术方式均未与并发症发生显著相关;相反,术前低血红蛋白和较高MELD评分为独立危险因素,提示即使在门脉压力得到控制后,肝病基础严重程度及全身储备仍主导围手术期风险。首年死亡亦以肝病相关为主而非肿瘤相关,进一步印证肝功能储备仍是长期预后的核心决定因素。风险评估方面,VOCAL-Penn评分在TIPS后人群中仍保持良好预测能力,且于减压后重新计算可更准确反映真实手术风险,这一发现对围手术期再分层具有重要实践意义。
从卫生经济学角度看,尽管U.N-TIPS带来额外初始成本,但若其能够促成根治性切除并减少门静脉高压相关并发症,总体上可能具有成本效益优势,尤其是在代偿期但围手术期高风险患者中。然而,长期随访仍需警惕分流相关远期并发症,对于肿瘤长期缓解且肝功能稳定的患者,个体化分流减径或关闭策略值得进一步探索。
综上,U.N-TIPS通过在血流动力学改善与分流安全性之间实现更优平衡,显著拓展了合并CSPH的肝硬化患者接受肝外恶性肿瘤根治性手术的可能性。本研究提示,门脉减压策略不仅能够重塑围手术期风险分层,而且有望动摇传统“CSPH即手术禁忌”的治疗范式。然而,肝病基础严重程度仍是决定长期预后的关键因素。未来亟需更大样本、前瞻性对照研究,以进一步明确该策略的长期生存获益、成本效益及其在多学科肿瘤管理体系中的最佳定位。
原文链接:Saltini D, Roccarina D, Senzolo M, et al. Neoadjuvant Under-Dilated TIPS: Expanding Surgeries for Extrahepatic Malignancies in Patients With Cirrhosis and CSPH. Liver Int. 2026;46(1):e70473. doi:10.1111/liv.70473

翻译&解读
雷甜甜
四川大学华西医院日间手术中心主治医师
四川大学华西医院消化内科,四川大学华西临床医学院博士研究生

专家简介
罗薛峰
四川大学华西医院消化内科
医学博士、副教授、博士研究生导师






