在肿瘤治疗领域,KRAS基因突变一直是科学家们想要攻克却又屡屡受挫的“硬骨头”。这个在1982年就被发现的致癌基因,因其特殊的蛋白结构和复杂的信号通路,在长达四十年的时间里被公认为“不可成药”靶点。
然而,随着医学技术的飞速发展,这一困境正在被打破。继针对KRAS G12C突变(俗称“12C”)的药物成功上市后,针对另一个常见突变亚型——KRAS G12V(俗称“12V”) 的研究也取得了突破性进展。
今天,无癌家园小编要为大家介绍的就是一款专门针对KRAS G12V突变的新型在研药物——XP001,以及它正在进行的针对肠癌和肺癌患者的临床招募。
揭秘KRAS G12V:那个让癌细胞"永动机"化的"失控开关"KRAS基因是人体内一种重要的信号传导分子,被誉为信号通路中的"开关"。在正常情况下,它在接收生长信号后启动细胞生长,完成任务后便"关闭"。但当KRAS基因发生突变时,这个开关就会卡在"持续开启"的状态,导致细胞不受控制地疯狂增殖,最终形成肿瘤。
我们可以这样理解:正常细胞就像一辆有刹车系统的汽车,需要加速时踩油门,需要停止时踩刹车。而KRAS突变,就等于刹车系统彻底失灵——油门一直踩到底,细胞永远处于"加速增殖"模式。
KRAS突变存在于约20%~30%的所有癌症中,是癌症中最常见的驱动基因突变之一。其中,KRAS G12V是仅次于G12D的高频突变亚型。
根据大规模泛癌种基因组分析,KRAS突变在胰腺导管腺癌中的发生率超过90%,在结直肠癌中约为40%,在肺腺癌中约为30%。而在这些突变中,G12D和G12V占据了胰腺癌的70%~75%。
这意味着,对于相当大一部分肺癌和肠癌患者来说,KRAS G12V突变是导致疾病发生和发展的"罪魁祸首"。
四十年魔咒终被打破:KRAS G12V为何长期"无药可医"?尽管针对KRAS G12C突变的药物(如索托拉西布Sotorasib、阿达格拉西布Adagrasib)已经获批上市,并在非小细胞肺癌中显示出良好的临床获益,但这些药物仅适用于G12C突变患者。
对于KRAS G12V突变患者,目前全球范围内尚未有任何一款靶向药物获批上市。 这背后有着深刻的科学原因:
KRAS G12V突变蛋白的分子结构与传统药物结合位点不匹配。KRAS蛋白表面光滑,几乎像一个"光溜溜的土豆",缺乏传统小分子药物可以结合的"深口袋"结构。尤其是G12V突变,由于其特定的氨基酸替换(甘氨酸变为缬氨酸),使得药物设计难度极高。
打个比方:传统靶向药像一把需要插入锁孔的钥匙,而KRAS G12V蛋白表面根本没有这个"锁孔"——这就是它长期"不可成药"的根本原因。
在临床实践中,KRAS G12V突变患者的治疗选择通常局限于化疗、免疫治疗或抗血管生成治疗。虽然这些治疗手段在一定程度上能够控制病情,但随着治疗时间的延长,耐药性的出现几乎不可避免。
一项2024年发表于ASCO的研究显示,在转移性非小细胞肺癌和结直肠癌中,KRAS G12V突变的高变异等位基因频率与更差的总生存期显著相关。在结直肠癌患者中,G12V高丰度患者死亡风险增加2.25倍;在非小细胞肺癌患者中,接受单纯化疗的G12V高丰度患者死亡风险增加1.93倍。
这些数据清晰地表明,KRAS G12V突变不仅是致癌的驱动因素,更是预后不良的重要标志。针对这一特定人群开发精准治疗药物,迫在眉睫。
XP001破局之道:从源头"剪断"致癌基因的智能导弹XP001是一种创新的小干扰RNA(siRNA)疗法,通过RNA干扰技术从源头上抑制KRAS G12V突变蛋白的表达。
作用机制:从源头"关闭"致癌基因
我们可以把KRAS基因想象成一个不断发出"生长、增殖"错误指令的"失控电台"。传统的靶向药物像是试图去堵住电台的喇叭,但往往效果有限。而XP001的工作原理则完全不同:
它利用特殊的LODER™聚合物基质包裹siRNA,通过超声内镜引导下的细针直接注射到肿瘤内部。一旦进入肿瘤组织,这种聚合物基质会像一个"智能缓释胶囊"一样,在数月内缓慢释放siRNA药物。
这些siRNA进入肿瘤细胞后,会像"分子剪刀"一样,特异性识别并切割KRAS G12V突变基因的信使RNA(mRNA)。没有了mRNA这个"生产模板",细胞就无法合成新的KRAS G12V突变蛋白。随着细胞内已有的突变蛋白逐渐降解,那条永不停歇的生长信号通路终于被"切断"。
临床前研究数据
在临床前研究中,XP001的前身siG12D-LODER已在胰腺癌模型中证实,通过靶向KRAS G12D/G12V等位基因,能够有效抑制肿瘤生长。这种局部递送策略不仅克服了系统性给药面临的体内降解和脱靶效应问题,还显著提高了肿瘤局部的药物浓度。
临床数据说话:针对G12V突变,生存期延长9.3个月XP001的临床开发基于坚实的科学证据。以下是最新公布的临床研究数据:
这是一项多中心、国际性的II期临床试验,共纳入59例局部晚期胰腺癌患者。研究分为两个队列:
队列1:37例患者,随机接受siG12D-LODER联合化疗(GnP方案)或单纯化疗
队列2:22例患者,接受siG12D-LODER联合标准化疗(FOLFIRINOX或GnP)
关键有效性数据
在全体人群中,siG12D-LODER联合化疗组的中位总生存期为22.7个月,对照组为21.9个月,差异未达到统计学显著性。
但是,当研究人员聚焦于携带KRAS G12D/G12V突变的患者时,令人振奋的结果出现了:
在KRAS G12D/G12V突变患者中,siG12D-LODER联合化疗组的中位总生存期达到22.7个月;而单纯化疗组的中位总生存期仅为13.4个月;这意味着生存期延长了9.3个月,死亡风险降低41%(HR 0.59)。
在客观缓解率方面:
G12D/G12V突变患者接受联合治疗后,客观缓解率达到63.6%;而单纯化疗组仅为20%。在队列2中,整体客观缓解率为31.6%,但在KRAS G12D/G12V突变患者中,客观缓解率高达57.1%,与队列1观察到的63.6%高度一致。
安全性数据
研究显示,siG12D-LODER的耐受性良好,未观察到剂量限制性毒性。在I/IIa期临床试验中,大多数患者(76%)达到疾病稳定,中位总生存期达到15个月。这种通过超声内镜直接将药物递送至肿瘤内部的创新方式,有效避免了系统性给药常见的全身性副作用。
最新进展
基于II期研究的积极结果,研究团队正在设计III期确证性研究。与此同时,新一代的siRNA候选药物SIL204正在开发中,它能够靶向更广泛的KRAS突变谱,包括G12D、G12V、G12R、Q61H和G13D等,有望覆盖更多患者。
真实病例:从无药可医到重获新生
在这一部分,我们将分享几个真实的病例。需要说明的是,这些病例分别采用了不同的治疗策略——有前面介绍的XP001 siRNA疗法,也有下面将要介绍的mRNA肿瘤疫苗联合免疫治疗。虽然技术路径不同,但它们共同指向一个核心:精准靶向KRAS G12V突变,正在改写晚期肿瘤患者的命运。
病例1:晚期非小细胞肺癌患者的多发转移病灶显著缓解(mRNA疫苗策略)
*(注:此病例为mRNA疫苗联合PD-1抑制剂治疗策略)*
这是一位69岁的男性患者,确诊为晚期非小细胞肺癌。诊断时,他的双肺已经出现多处转移灶,纵膈淋巴结也受到累及。基因检测显示患者携带KRAS G12V突变。
患者在接受一线化疗(部分病例背景中提到曾接受6个周期的化疗联合免疫治疗)后,疾病仍然进展,出现了化疗耐药,属于典型的"后线治疗"人群。面对传统治疗失败后的困境,治疗选择非常有限。
在医生建议下,患者加入了针对KRAS G12V突变的mRNA疫苗临床试验,接受疫苗联合PD-1抑制剂治疗。
治疗的过程需要耐心,但结果令人振奋。经过9个周期的治疗,影像学评估显示:患者的右肺病灶几乎完全消失,左肺及淋巴结的病灶也显著缩小,整体疗效达到部分缓解(PR),且没有出现明显不良反应。
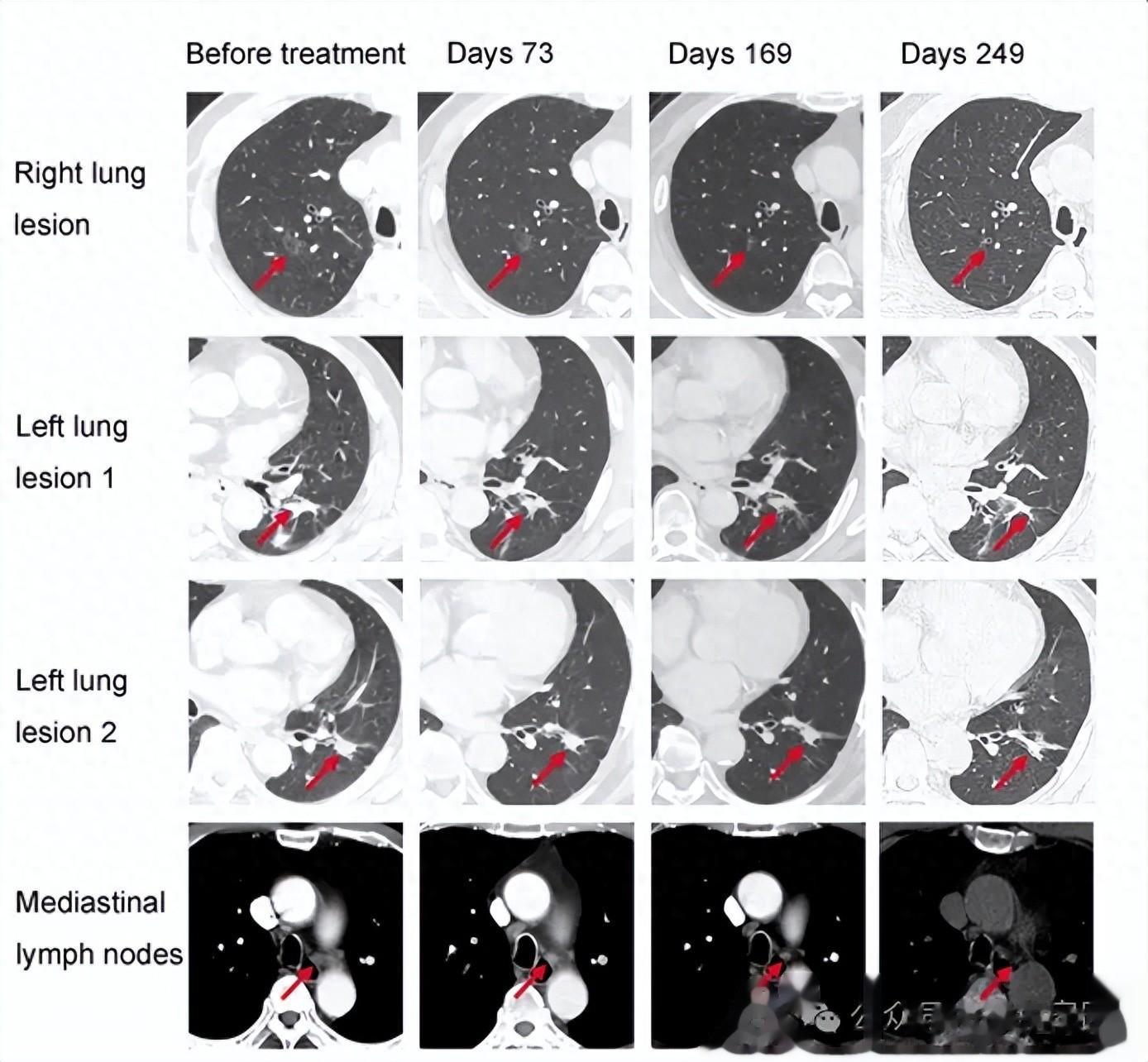
患者002疫苗接种前后多发肿瘤病灶的CT对比(侵删)
这个案例尤其值得关注的是,这位患者在接受治疗前已经出现化疗耐药。但精准靶向KRAS G12V的免疫策略仍然为他带来了显著的临床获益。这表明,即使是在传统治疗失败后,针对KRAS G12V突变的精准治疗仍然值得尝试,为耐药患者带来了新的希望。
病例2:86岁高龄胰腺癌患者的生命奇迹(mRNA疫苗策略)
(注:此病例为mRNA疫苗联合PD-1抑制剂治疗策略,发表于《Cell Research》)*
这是一位86岁的女性患者,因胆道梗阻就诊,被确诊为局部晚期胰腺癌。由于高龄和较差的体能状态(ECOG评分为3分,意味着患者每天有超过50%的时间需要卧床),她既没有手术机会,也无法耐受传统化疗。面对这样的困境,任何积极治疗似乎都成了奢望。
然而,基因检测结果显示患者携带KRAS G12V突变。在充分评估后,医疗团队决定尝试针对KRAS G12V的mRNA疫苗联合PD-1抑制剂帕博利珠单抗这一创新方案。
令人惊喜的是,在首次疗效评估时,患者的胰头肿瘤明显缩小,达到部分缓解(PR)。对于一个86岁、ECOG 3分、原本已无任何治疗选择的患者来说,这一结果堪称奇迹。这不仅证明了mRNA疫苗策略在高龄、体弱患者中的可行性,也为更多类似处境的患者带来了希望。
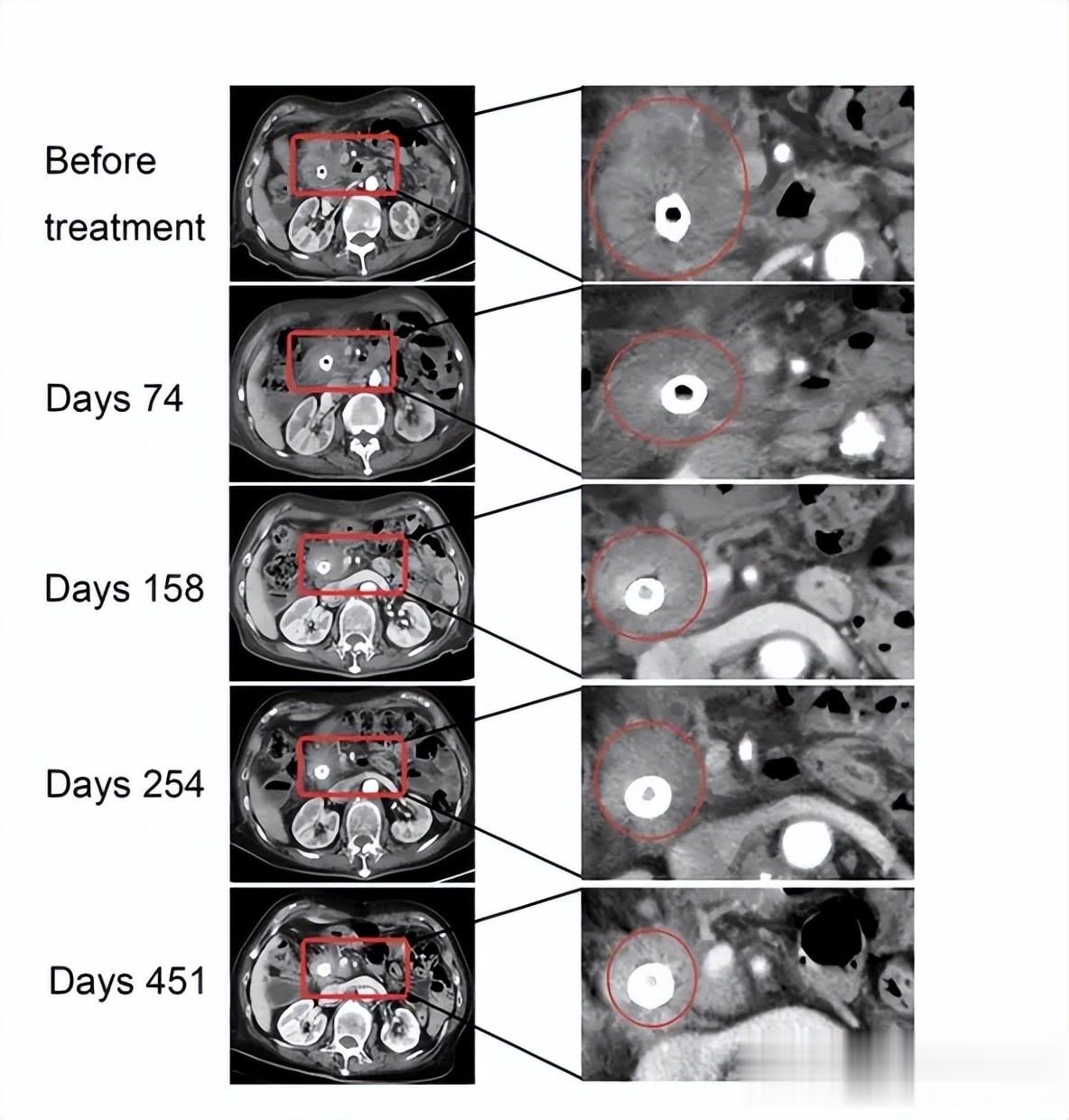
患者001疫苗治疗前后肿瘤病灶的CT对比(侵删)
病例3:KRAS G12V突变肺癌的个体化探索(联合用药策略)
(注:此病例为泛ERBB抑制剂联合抗血管生成治疗策略)
另一例报告发表于《Pneumonia》期刊,描述的是一位49岁的不吸烟女性患者,最初因肺部阴影就诊,术后病理确诊为肺腺癌,基因检测显示KRAS G12V突变。
在接受手术和辅助化疗后,患者的肿瘤标志物CEA水平再次升高,CT显示新的病灶出现。尽管后续接受了多线化疗、免疫治疗和抗血管生成治疗,但疾病仍持续进展。
面对治疗困境,医疗团队制定了个体化的阿法替尼联合贝伐珠单抗和长春瑞滨方案。令人欣慰的是,这一方案使患者达到了持续14个月的疾病稳定,且无明显不良反应。
虽然这个案例使用的是泛ERBB抑制剂而非直接靶向KRAS G12V的药物,但它揭示了一个重要事实:KRAS G12V突变肿瘤对精准治疗存在潜在敏感性,值得我们投入更多努力去寻找最佳的靶向策略。
目前无癌家园正有多款癌症疫苗的临床试验正在进行中:
主要为晚期恶性实体肿瘤(包括但不限于晚期实体瘤/非小细胞肺癌、晚期胰腺导管腺癌、卵巢癌、胸膜间皮瘤、前列腺癌、肝癌、乳腺癌、膀胱癌等)。
从病例到希望:这些真实故事告诉我们什么?
上述病例中,分别代表了不同类型、不同年龄、不同治疗背景的KRAS G12V突变患者。他们中有化疗耐药的中老年肺癌患者,也有高龄体弱、无任何治疗选择的胰腺癌患者。尽管情况各异,但他们都传递了几个重要信息:
第一,精准治疗没有"年龄歧视"。 86岁、ECOG 3分的高龄患者,同样可以从靶向治疗中获益。在精准医学时代,体能状态不应成为放弃治疗的唯一理由,基因型才是更重要的决策依据。
第二,后线治疗不等于无效治疗。 即使已经对多种传统治疗耐药,精准靶向策略仍可能带来显著疗效。对于化疗失败的KRAS G12V突变患者,参与临床试验不是"死马当活马医",而是科学、理性的主动选择。
第三,技术路线多样化为患者提供更多选择。小编重点介绍的XP001是siRNA技术路线,而上述两个病例采用的是mRNA疫苗联合免疫治疗策略。此外,CAR-T细胞疗法、泛RAS抑制剂、靶向蛋白降解剂等多种技术路径也正在齐头并进。这意味着,即使一种技术路线不适合某位患者,仍有其他选择可以尝试。
如果您或您的家人陷入非小细胞肺癌、肠癌的治疗困境,且尚未找到有效的解决方案,那么参与这项临床研究可能是一个值得考虑的选择。
主要入选标准:
年龄: ≥18周岁。
条件:A)肿瘤组织携带 KRAS G12V 突变的肠癌和肺癌(可接受研究者认可的既往12个月内的检测报告)。
B)不盲筛,认可既往G12v基因检测结果
C)切片:需要8-10张切片,新鲜切片8张,存量切片10张。肌肉注射,21天为一个周期。
D)肺癌:晚期非小细胞肺癌至少一线治疗病情稳定;MSS转移性晚期结直肠癌,至少经过二线或二线以上治疗(一线可推);
D)剂量扩展阶段要求至少1个能够有效呈递该抗原的HLA(HLA-A11:01、HLA-A03:01 、 HLA-A30:01 、 HLA-A68:01 、 HLA-C01:02 、HLA-C03:03、HLA-C03:04);
E)排除LNP(脂质纳米颗粒)过敏患者,既往对含有 LNP 的药物,mRNA-LNP 新冠疫苗等同类型传染病疫苗有过全身过敏反应的患者
多路并进:除了XP001,还有哪些新技术在瞄准G12V?
除了XP001的siRNA技术路线和上述病例中提到的mRNA疫苗策略外,针对KRAS G12V突变的多项创新疗法也取得了令人瞩目的进展:
1. CAR-T细胞疗法
2026年2月,皖南医学院第一附属医院在国际权威期刊《Science Advances》发表研究,成功研发出针对KRAS G12V/HLA-A*02:01靶点的CAR-T细胞。这种CAR-T细胞能够特异性识别并清除表达该靶点的肿瘤细胞,在多种动物模型中展现出良好的抗肿瘤活性和安全性[9]。
值得注意的是,HLA-A*02:01在亚洲人群中约占10%-20%,在欧美人群中高达30%-50%,这意味着该疗法有望惠及更广泛的患者群体[9]。
2. mRNA肿瘤疫苗
上海交通大学医学院附属瑞金医院在全球首次报告了针对KRAS G12V单靶点的mRNA肿瘤疫苗在实体瘤中的治疗效果。研究显示,KRAS G12V与亚洲人群中出现频率极高的HLA-A*11:01具有最强的结合亲和力和稳定性,因此相当一部分亚洲患者可能从这一疗法中获益[8]。
3. 泛RAS抑制剂
贝达药业在2025年AACR年会上报告了BPI-572270,一种强效的泛RAS抑制剂。在KRAS G12V和G12D的人胰腺癌小鼠模型中,低剂量每天口服给药一次即可实现肿瘤消退[10]。
4. KRAS靶向降解剂
同样来自国研新药BPI-585725是一种靶向蛋白降解嵌合体(PROTAC)分子,能够对包括G12V在内的多种KRAS突变展现出显著的降解能力。在动物模型中,单次给药可在肿瘤组织中维持有效浓度长达6天。
这些多样化的技术路线共同指向一个光明的未来:KRAS G12V突变将不再是"不可成药"的禁区。
行动起来:你的基因检测报告,可能藏着救命线索
对于肺癌、肠癌和胰腺癌患者来说,面对KRAS G12V这一曾经令人绝望的靶点,无癌家园可以给出更加积极的建议:
首先,明确自己的基因状态。 如果尚未进行过基因检测,或者只做过少数几个位点的检测,建议考虑使用高通量测序技术进行全面检测。KRAS G12V虽然是常见突变,但并非在所有患者中都存在,精准治疗的前提是精准诊断。
其次,关注新药临床研究动态。 药物从研发到上市往往需要数年时间,而临床试验为符合条件的患者提供了提前获得创新疗法的宝贵机会。XP001及相关研究的招募信息,可能是您或家人的重要转机。
最后,保持信心。 从1982年发现KRAS基因,到2021年首个KRAS G12C抑制剂获批,这条路走了近40年。如今,针对G12V的多种技术路线已经进入临床或临床前研究后期,我们有理由相信,在不远的将来,针对这一靶点的精准治疗将成为现实。
本文为无癌家园原创