编者按
国内大型真实世界研究iCaReMe China显示,我国71.5%的2型糖尿病(T2DM)患者接受了联合降糖治疗,二甲双胍与钠-葡萄糖协同转运蛋白2抑制剂(SGLT2i)是最常用的两种降糖药物[1]。临床上联合治疗方案多样且各有特点,如何依据患者特征选择适配方案成为关键问题。近期,一项系统评价和荟萃分析研究[2]比较了SGLT2i联合二甲双胍与其他含二甲双胍的两联方案在疗效及安全性方面的差异,为临床医生制定T2DM治疗方案提供了重要的循证参考。

结果
降糖:总体而言,SGLT2i+二甲双胍与其他两联治疗方案在降低糖化血红蛋白(HbA1c)方面的疗效相当;亚组分析显示,在第52周时,该方案较二肽基肽酶-IV抑制剂(DPP-4i)+二甲双胍可降低HbA1c 0.11%。
体重降低:在第52周时,SGLT2i+二甲双胍较其他两联治疗方案体重降低2.59 kg;亚组分析可见,在第24周、52周时,该方案较DPP-4i+二甲双胍分别体重降低1.93 kg、2.38 kg。
安全性:各类方案的总体严重不良事件风险相当;第52周时,SGLT2i+二甲双胍的低血糖风险较其他两联方案降低73%,较磺脲类药物+二甲双胍降低90%,低血糖安全性优势突出。
一、研究背景和目的
据国际糖尿病联盟(IDF)最新数据[3],2024年全球成人T2DM患者约5.59亿,预计到2050年将攀升至8.53亿,其中中国作为糖尿病第一大国,2024年成人患者已达1.48亿。在此背景下,选择最优的药物治疗方案,实现血糖控制与并发症预防的双重目标,是临床医生和患者共同关注的焦点。
近年来,早期联合治疗理念在国内外指南中日益凸显,获多个“A级推荐”,成为T2DM的重要降糖策略。2026年美国糖尿病协会(ADA)《糖尿病诊疗标准》建议[4]:成人T2DM患者起始治疗时即可考虑联合治疗,以缩短实现个体化治疗目标的时间(A级推荐)。中华医学会糖尿病学分会(CDS)《中国糖尿病防治指南(2024版)》指出[5]:早期良好的血糖控制具有重要意义,早期联合是实现良好血糖控制的重要手段(A)。早期、合理联合应用机制互补的降糖药物利于T2DM患者实现早期血糖达标并长期维持(A)。
SGLT2i作为新型口服降糖药,通过抑制肾脏近端小管对葡萄糖的重吸收,增加尿糖排泄,实现不依赖胰岛素的降糖效果,且大量循证医学证据证实SGLT2i具有显著的心肾保护作用,可降低心血管死亡率、延缓慢性肾脏病进展、减少心力衰竭住院风险等[6-9]。基于此,美国临床内分泌医师协会(AACE)、ADA、中国糖尿病指南均推荐,对于合并动脉粥样硬化性心血管疾病、心力衰竭或慢性肾脏病的T2DM患者,应优先选择SGLT2i等[4-5,10]。
基于以上优势,SGLT2i早期联合二甲双胍成为国内外指南推荐的“一线”*口服降糖方案,该联合方案可通过T2DM多重病理生理机制及多个靶点,实现“1+1>2”,降糖兼顾心肾保护,给患者带来诸多获益,尤其固定复方制剂更具简化方案、提升治疗依从性等优势。然而,尽管SGLT2i联合二甲双胍的临床应用日益广泛,但与其他含二甲双胍的两联方案相比,仍缺乏系统性的比较证据。
二、研究方法
该研究采用系统评价与荟萃分析(MA)方法,全面检索MEDLINE、Embase、Cochrane系统评价数据库及2021~2023年ADA/EASD会议摘要。纳入标准聚焦于平行随机对照试验(RCT),要求研究对象为成人T2DM患者,干预措施为SGLT2i联合二甲双胍对比其他含二甲双胍的口服两联方案,治疗持续时间不少于24周,并报告相关疗效和安全性结局。
主要疗效指标:第24周和/或52周时,HbA1c、体重较基线的变化,治疗失败率;主要安全性指标涵盖低血糖、尿路感染(UTI)、生殖器感染、心肌梗死、全因死亡、总体严重不良事件等。
三、研究结果
经过严格筛选,最终纳入23项RCTs,共36篇发表文献。其他含二甲双胍的口服两联方案包括联合DPP-4i、磺脲类药物或胰高糖素样肽-1受体激动剂(GLP-1RA)等。
01
疗效:总体与其他方案相当,部分终点优势显著
1.血糖控制:第24周和第52周时,SGLT2i+二甲双胍与其他含二甲双胍的两联治疗方案降低HbA1c的总体疗效相当(第24周、52周的平均差异分别为:0.09%、0.01%,图1)。

图1. 第24周(a)、52周(b)组间HbA1c的平均差异
亚组分析显示,与DPP-4i+二甲双胍相比,SGLT2i+二甲双胍在第24周时无显著差异,但在第52周时显示出HbA1c降低优势(平均差异:-0.11%,95%CI:-0.19~-0.02);与磺脲类药物+二甲双胍比较,组间在第52周时无显著差异。
2.体重管理:体重管理是T2DM综合治疗的重要组成部分,对于改善胰岛素抵抗、降低心血管风险具有独立价值。该研究发现,第24周时SGLT2i+二甲双胍与其他两联方案的体重无显著差异,但第52周时较其他方案平均体重降低2.59 kg(95%CI:-4.42~-0.77,图2a)。其中,与DPP-4i+二甲双胍相比,该方案在第24周平均体重降低1.93 kg,且这一优势在第52周达到2.38 kg(图2b)。
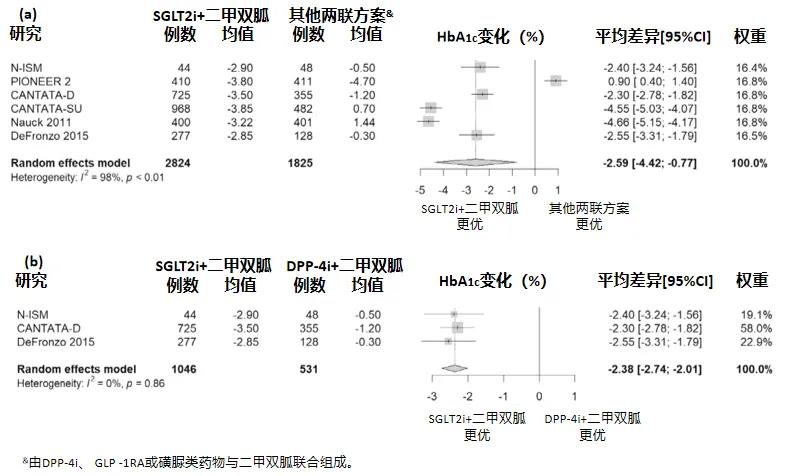
图2. 与其他两联方案(a)、DPP-4i+二甲双胍(b)比较,52周的体重变化
3.治疗失败率:第52周时,SGLT2i+二甲双胍与其他两联方案的治疗失败风险无显著差异(RR:0.72;95%CI:0.49~1.04),证实该方案的治疗稳定性。
02
安全性特征:低血糖风险显著降低,尿路感染风险与其他联合方案无差异
1.低血糖:低血糖是降糖治疗中最受关注的不良事件,不仅直接影响患者生活质量,还可能诱发心脑血管事件,甚至危及生命。该荟萃分析显示,第52周时,SGLT2i+二甲双胍的低血糖风险较其他方案显著降低73%(RR:0.27,95%CI:0.09~0.84,图3a)。在针对磺脲类药物的亚组分析中,SGLT2i的优势更为突出:低血糖风险降低达90%(RR:0.10,95%CI:0.07~0.16,图3b)。

图3. 低血糖风险
2.心血管与死亡相关指标:心肌梗死风险方面,SGLT2i+二甲双胍较其他方案呈数值降低趋势(RR:0.58,95%CI: 0.16~2.07),提示心血管获益趋势。
3.感染相关风险:作为SGLT2i的类效应,尿路感染和生殖器感染风险一直备受关注。该研究发现,SGLT2i联合二甲双胍的尿路感染风险与其他方案相比虽有数值升高(RR:1.22,95%CI:0.94~1.58),但无统计学差异,且与DPP-4i+二甲双胍的风险完全相当(RR:1.00;95%CI:0.69~1.45)。这表明在规范使用和充分患者教育的前提下,尿路感染风险可控。
需关注的是,SGLT2i+二甲双胍的生殖器感染风险显著升高(风险比:5.08,95%CI:3.49~7.38),该结果与药物作用机制直接相关——尿糖排泄增加为泌尿生殖道微生物繁殖提供了有利环境。但现有共识表明[11],此类感染多为轻至中度,可通过标准抗菌治疗有效控制,通常无需停用SGLT2i。
4.其他安全性指标:在全因死亡、卒中、腹泻、总体严重不良事件等指标上,SGLT2i联合二甲双胍与其他两联方案均无显著差异,显示出良好的总体安全性。
四、研究讨论与总结
该项研究结果显示,SGLT2i联合二甲双胍与其他含二甲双胍的口服两联方案在长期血糖控制方面疗效相当,且与DPP-4i联合二甲双胍比较,SGLT2i方案进一步降低HbA1c,这一差异可能源于两类药物的作用机制不同:SGLT2i通过直接增加尿糖排泄、轻度利尿等作用实现降糖、减重效果,而DPP-4i的降糖作用则是间接的,通过调节肠促胰素增加胰岛素分泌并减少胰高血糖素释放,效果相对温和,且呈体重中性的药理学特征,无减重作用[12,13]。
在安全性方面,SGLT2i联合二甲双胍在第52周时低血糖风险显著降低73%~90%,远超临床认为的50%最小临床重要差异(MCID)阈值[14]。这一优势对于特殊人群具有重要意义:对于老年患者、肾功能不全患者、合并心血管疾病或从事高危职业(如驾驶员、机械操作者)的糖尿病患者,选择SGLT2i联合二甲双胍可显著降低低血糖相关风险。此外,泌尿系统感染相关风险的管理是SGLT2i临床应用的重点关注内容。临床实践中,需在治疗前向患者充分告知感染风险,指导其保持泌尿生殖道清洁干燥、多饮水、避免憋尿等预防措施。
综上所述,在T2DM治疗日益强调个体化和综合管理的新时代,SGLT2i联合二甲双胍凭借其确切的降糖疗效、突出的低血糖安全性和潜在的心肾保护作用,已成为联合治疗的重要选择。相较于二者的自由联合,近些年获批上市的SGLT2i/二甲双胍缓释片这类固定复方制剂具有简化治疗、降糖效果平稳、助力提高治疗依从性等优势,为全球数亿T2DM患者的规范治疗与长期管理带来切实获益。
注:* T2DM患者合并心肾风险或心肾疾病,SGLT2抑制剂和二甲双胍是国内外权威指南中推荐的初始联合治疗之一。2023 AACE指南推荐二甲双胍为一线降糖治疗药物;2025 ADA、2024CDS指南提出针对T2DM心肾风险管理均明确将SGLT2i作为口服治疗的一线选择。
仅供医疗卫生专业人士参考,不得转发或分享非医疗卫生专业人士。不得用于推广目的,若涉及具体药物使用,请参考相关药物说明书,阿斯利康公司不建议您将产品超说明书使用。
参考文献
1.Yang W, et al. The treatment patterns of patients with type 2 diabetes in China-results from iCaReMe China Registry.ICDM 2024.
2.Ma YH, et al. Endocrinol Diabetes Metab . 2026 Mar;9(2):e70176. doi: 10.1002/edm2.70176.
3.https://diabetesatlas.org/resources/idf-diabetes-atlas-2025/.
4.American Diabetes Association Professional Practice Committee for Diabetes. Diabetes Care. 2026; 49(Suppl. 1): S1-S362.
5.中华医学会糖尿病学分会. 中华糖尿病杂志. 2025; 17(1): 16-139.
6.McEwan P, et al. Nephrol Dial Transplant. 2024; 39(12): 2040-2047.
7.Wanner C, et al. Circulation. 2018; 137(2): 119-129.
8.Wiviott SD, et al. N Engl J Med. 2019; 380(4): 347-357.
9.Zinman B, et al. N Engl J Med. 2015; 373(22): 2117-2128.
10.Samson SL, et al. Endocr Pract. 2023; 29(5): 305-340.
11.Gorgojo-Martínez JJ, et al. Journal of Clinical Medicine. 2024; 13(21): 6509.
12.Mishriky B, et al. Diabetes Metab. 2018; 44(2): 112-120.
13.Centre for Reviews and Dissemination. Systematic reviews: CRD's guidance for undertaking reviews in health care. 2008; https://www.york.ac.uk/media/crd/Systematic_Reviews.pdf. Accessed 3 July 2025.
14.Dankers M, et al. Pharmacol Res Perspect. 2021; 9(3): e00750.
CN-179672
2026-09-11